干细胞治疗系统性斑狼疮的基础和87例临床研究
系统性红斑狼疮(SLE) 是一种异质性的慢性自身免疫性疾病,血清中出现以抗核抗体(ANA)为代表的多种自身抗体和多系统受累是SLE的两个主要临床特征。
研究人员等认为遗传易感性与外界因素如药物、紫外线、感染、压力等共同参与了SLE发病。尽管影响因素不同,但基本和最终的途径是大量免疫细胞(包括T细胞、B细胞和单核细胞系)的畸变,导致T细胞缺陷、多克隆B细胞活化、产生自身抗体和免疫复合物的形成。
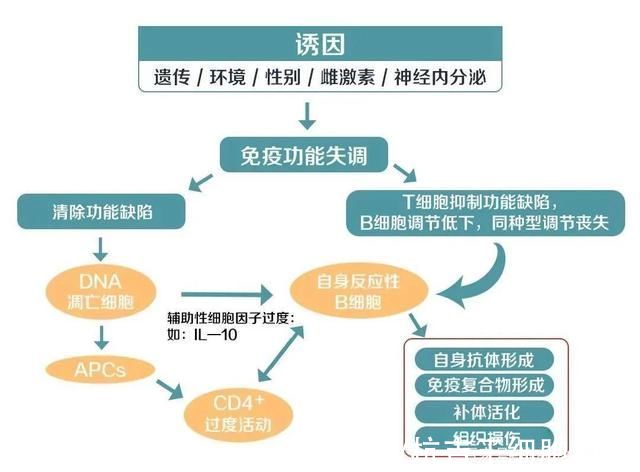
目前关于红斑狼疮的常规治疗方法有:抗炎药、抗疟药、糖皮质激素、免疫抑制剂等,主要针对病症-抗原-抗体复合物沉积导致的炎症,但目前没有针对病因的治疗方案,而且这些治疗都有明显的副作用。
间充质干细胞(MSC)是一种来源广泛的干细胞,具有多向分化功能和免疫调节功能。前期已从动物实验、临床试验等多方面对MSC移植进行了研究,已初步证实了MSC移植治疗SLE的有效性和安全性。
专家表示MSC可分泌多种细胞因子,如巨噬细胞集落刺激因子、IL一6和血管内皮生长因子等,参与造血调控、促血管生成及免疫调控等多种作用。鉴于这些优点和它极低的免疫原性,MSC已经被认为是一种理想的细胞治疗、组织工程和基因治疗的新型靶细胞。
2004年,LeBlanc等报道了首例异基因MSC移植成功治疗类固醇治疗无效的严重的移植物抗宿主病(GVHD)。目前美国食品药品监督管理局已经批准MSC作为急性GVHD治疗的一线药物用于临床。
MSC移植治疗SLE的机制
目前认为主要机制包括以下4方面
MSC归巢:有研究发现MRL/lpr小鼠移植后,很快就能在肾、肺、肝、脾等组织检测到CFSE标记的UC-MSC,在24h达到最高水平,并持续1周。静脉输注MSC11周后仍然能在肾脏检测到移植的MSC。
MSC对T细胞的调控:MSC移植疗效主要依赖于MSC对各种免疫细胞的调节作用,其中最重要的是对T细胞的调控。
MSC对B细胞的调控:狼疮小鼠经MSC移植后,血清IgG和IgM水平显著降低;狼疮患者经MSC移植后,血清ANA、抗ds-DNA抗体水平显著降低,都表明MSC可调节B细胞功能。
MSC对巨噬细胞的调控:巨噬细胞存在于所有组织中,具有极大的可塑性和功能多样性,是免疫应答、组织修复、维持机体稳态的关键调节。
基础研究
MSC联合HSC移植治疗狼疮小鼠HSCT的基本 原理是重建免疫系统,但是自体HSCT面临高复发的风险,而异体MSC移植易出现移植排斥反应。所以有研究者尝试MSC联合HSC移植治疗狼疮小鼠。
MRLflpr小鼠经静脉输注不同混合比例的HSC和MSC(分别为1:5,1:1,5:1,1:0),8周后,移植细胞比例为5:1组的狼疮小鼠与仅接受HSCT组的小鼠相比,蛋白尿和血清肌酐水平的降低、肾组织病理学的改变更明显,移植物抗宿主反应的发生率更低阁。这些结果表明,MSC可以明显提高HSCT治疗MRL/lpr小鼠的疗效。
临床案例
在一项纳入87例难治性SLE患者的Ⅱ期临床研究中,59%的患者在移植前3d接受CYC[10mg/(kg·d)]治疗以期抑制淋巴细胞反应,41%的患者由于严重的基础疾病未接受CYC治疗。
69例患者接受了1次MSC移植,18例患者接受了多次MSC移植。平均随访27个月后,患者的总生存率为94%,且生存率与病程、 初始SLEDAI评分、MSC的来源或CYC预处理方案均无关。缓解时间3-24(9.4)个月,总复发率为23%(20/87), 5例死于非移植相关事件。同时,该研究还对BM-MSC和UC-MSC的移植疗效进行对比,发现后者的疗效更优。

MSC移植的安全性和展望
已有MSC移植狼疮后的一些小样本的长期安全性研究,数据显示MSC移植后无移植相关死亡,血清肿瘤相关标志物包括甲胎蛋白、癌胚抗原、糖抗原(CA)155和CAl9-9无升高,提示狼疮患者MSC移植的安全性。国外多个随机对照临床试验的统计学结果发现MSC治疗组和对照组的感染率没有差异,明确提出MSC治疗不会增加感染的风险。
随着研究的进展,干细胞疗法在治疗其他自身免疫性疾病方面也逐渐崭露头角。最终解决部分慢性病、组织修复与再生方面的问题。未来有望从根本上改变目前的医疗困局。